 大阪地方裁判所第21民事部(松川充康裁判長)は、本年(令和8年・2026年)3月3日、存続期間の延長登録がされた医薬用途発明に係る特許権に基づく差止請求を棄却する判決を言い渡しました。本判決は、先行処分(分量24μg)に基づく延長登録の存続期間満了後において、当該先行処分とは分量のみが異なる後行処分(分量12μg)に基づく延長登録がされた医薬用途発明に係る特許権の効力範囲をどのように解釈すべきかという問題について一定の判断を示したものです。なお、本判決に対しては、原告により控訴が提起されています。
大阪地方裁判所第21民事部(松川充康裁判長)は、本年(令和8年・2026年)3月3日、存続期間の延長登録がされた医薬用途発明に係る特許権に基づく差止請求を棄却する判決を言い渡しました。本判決は、先行処分(分量24μg)に基づく延長登録の存続期間満了後において、当該先行処分とは分量のみが異なる後行処分(分量12μg)に基づく延長登録がされた医薬用途発明に係る特許権の効力範囲をどのように解釈すべきかという問題について一定の判断を示したものです。なお、本判決に対しては、原告により控訴が提起されています。
ポイント
本判決の骨子
概要
裁判所は、被告製品は本件各発明の技術的範囲に属するが、延長特許権の効力は被告製品の生産・譲渡等に及ばないと判断しました。すなわち、本件においては、特許発明の技術的範囲の属否に関する第1ステップはクリアしたものの、延長特許権の効力に関する第2ステップをクリアできず、延長特許権の侵害は成立しないと判断されたものです。
特許発明の技術的範囲と被告製品について(第1ステップ)
- 結論
・被告製品は本件各発明の技術的範囲に属する。
- 理由
・技術常識等に照らすと、「慢性便秘症(器質的疾患による便秘を除く)の改善」を用途とする被告製品は、本件各発明1の構成要件である「哺乳類対象における機能性胃腸疾患による腹部不快感の処置のための」及び「機能性胃腸疾患の処置のための」、並びに本件各発明2の構成要件である「オピオイド化合物または抗コリン作用薬による薬物誘発性便秘処置用」の各要件を充足する。
・特許出願過程を参酌しても、出願当時の特許請求の範囲から「便秘の処置」を意識的に除外したとまでは解することができない。
存続期間が延長された特許権の効力について(第2ステップ)
- 結論
・後行処分(分量12μg)に基づく延長特許権の効力は、先行処分(分量24μg)の後発医薬品である被告製品には及ばない。
- 理由
・延長特許権の効力範囲は、延長登録の範囲・単位についての解釈と整合的で、特許権者と第三者との衡平にも適うものであるかという観点で検討すべきである。
・成分、分量、用法、用量、効能及び効果をもって、物としての特定要素とし、これを異にする医薬品については、それぞれごとに、特許権の存続期間延長の可否及びその期間の長短を審査、査定する、というベバシズマブ最高裁判決が示した「短冊化」された延長登録の範囲・単位に照らすと、延長特許権の効力範囲についても、当該短冊化された範囲内にとどまると解するのが整合的である。
・延長特許権の効力範囲は、特許発明の内容に基づき、その内容との関連で、政令処分において定められた「成分、分量、用法、用量、効能及び効果」によって特定された「物」と対象製品との技術的特徴及び作用効果の同一性を比較検討して、当業者の技術常識を踏まえて判断すべきである(オキサリプラチン知財高裁判決参照)。
・以上を踏まえると、延長特許権の効力範囲は、延長登録の範囲・単位と必ずしも一致するものではなく、存続期間の延長登録の範囲・単位と抵触しないという制約の中で解釈されるべきである。
・先行処分の対象とする物と成分、分量、用法、用量、効能及び効果として同一の物は、後行する延長登録の理由となった政令処分の対象とする物と実質同一ではなく、その生産・譲渡等にまでは効力が及ばない。
判決概要
| 裁判所 | 大阪地方裁判所第21民事部 |
|---|---|
| 判決言渡日 | 令和8年3月3日 |
| 事件番号 事件名 |
令和7年(ワ)第10786号、同第10790号 特許権侵害差止請求事件 |
| 裁判官 | 裁判長裁判官 松 川 充 康 裁判官 阿波野 右 起 裁判官 西 尾 太 一 |
解説
特許法における延長登録制度について
特許制度は、発明の公開と引き換えに、特許法第67条第1項において、特許出願日から20年間の独占権を認めることで、産業の発展に寄与することを目的としています。
(存続期間)
第六十七条 特許権の存続期間は、特許出願の日から二十年をもつて終了する。
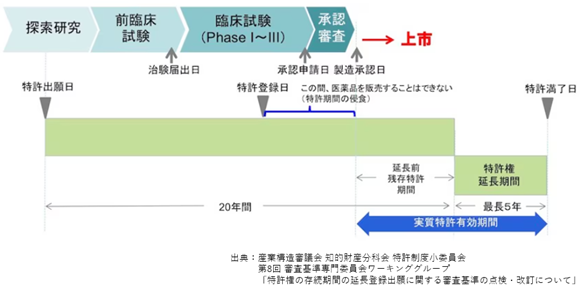
しかし、医薬品等の分野においては、安全性確保のための政府による許認可に長期間を要するため、その間、特許権者は権利を十分に活用できないという問題があります。すなわち、下図のとおり、医薬品に関する発明が特許登録されたとしても、製造販売承認を得るまでは当該医薬品を販売等することができず、結果として特許期間が実質的に侵食されることになります。このような事情を踏まえ、特許法は、政令で定める処分により特許発明の実施が制限されていた期間について、5年を上限として特許権の存続期間を延長できる制度を設けています(特許法第67条第4項)。
(存続期間)
第六十七条
(略)
4 第一項に規定する存続期間・・・は、その特許発明の実施について安全性の確保等を目的とする法律の規定による許可その他の処分であつて当該処分の目的、手続等からみて当該処分を的確に行うには相当の期間を要するものとして政令で定めるものを受けることが必要であるために、その特許発明の実施をすることができない期間があつたときは、五年を限度として、延長登録の出願により延長することができる。
このように、延長登録制度は、特許権者が本来享受し得た実施期間を回復することを目的として設けられた制度です。
延長登録の範囲・単位について
従前の特許庁実務
延長登録を受けるためには、その特許発明の実施に当たり、政令で定める処分を受ける必要があったと認められることが要件とされています(特許法第67条の7第1項第1号)。
(存続期間)
第六十七条の七
審査官は、第六十七条第四項の延長登録の出願が次の各号のいずれかに該当するときは、その出願について拒絶をすべき旨の査定をしなければならない。
一 その特許発明の実施に第六十七条第四項の政令で定める処分を受けることが必要であつたとは認められないとき。
(略)
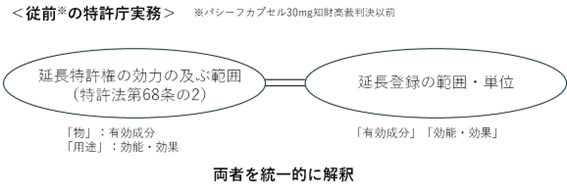
本号における「その特許発明の実施」の解釈は、延長特許権の効力範囲との関係で問題となり得ます。いわゆる「パシーフカプセル30㎎知財高裁判決」(知財高判平21年5月29日平成20年(行ケ)第10460号)以前の特許庁実務では、既に延長登録を受けた特許権の効力範囲と重複する部分については新たな延長登録を認めないようにする観点から、延長特許権の効力が及ぶ範囲(特許法第68条の2)と延長登録の範囲・単位とを統一的に解釈する必要があると考えられていました(中山ら編(2017)『新・注解 特許法 第2版 中巻』:青林書院)。
(第六十七条第四項の規定により存続期間が延長された場合の特許権の効力)
第六十八条の二
第六十七条第四項の規定により同条第一項に規定する存続期間が延長された場合・・・の当該特許権の効力は、その延長登録の理由となつた第六十七条第四項の政令で定める処分の対象となつた物(その処分においてその物の使用される特定の用途が定められている場合にあつては、当該用途に使用されるその物)についての当該特許発明の実施以外の行為には、及ばない。
そして、同条における「物」及び「用途」の意義については、存続期間延長制度の趣旨が、新たな有効成分又は効能・効果を有する医薬品の開発インセンティブを確保する点にあることから、「物」は「有効成分」を、「用途」は「効能・効果」を意味すると解されていました。そのため、延長登録の範囲・単位についても、同様に、「有効成分」、「効能・効果」を基準とするものと考えられており、先行処分に係る医薬品と有効成分及び効能・効果が同一の医薬品について後行処分がされた場合には、その特許発明の実施に当該政令処分を受ける必要があったとは認められず、延長登録は認められていませんでした。
パシーフカプセル30㎎知財高裁判決後の審査実務(短冊化)
しかし、その後の「パシーフカプセル30mg知財高裁判決」では、延長特許権の効力範囲と延長登録の範囲・単位とを統一的に解釈する考え方を否定し、延長登録要件の判断において、先行処分に基づく延長特許権の効力範囲は常に直接関係するものではないことを示しました。
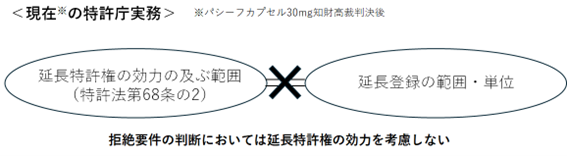
さらに、その後のいわゆる「ベバシズマブ知財高裁判決」(知財高判大合議平成26年5月30日平成25年(行ケ)第10195号)において、知財高裁は、特許法第67条の7第1項第1号に基づく拒絶要件に関し、医薬品の成分を対象とする特許については、成分によって禁止が解除される「特許発明の実施」の範囲は、成分、分量、用法、用量、効能及び効果によって特定される医薬品の製造販売等の行為であることを明確にするとともに、当該拒絶要件の判断においては延長特許権の効力を考慮しないことを示しました。
また、同判決の上告審である「ベバシズマブ最高裁判決」(最判平成27年11月17日・平成26年(行ヒ)第356号)は、後行処分に係る医薬品の製造販売等が先行処分に係る医薬品の製造販売等を包含する場合には、同号により拒絶される旨を判示しています。さらに、このような包含関係の有無は、特許発明の種類や対象に照らし、医薬品としての実質的同一性に直接関わる審査事項、すなわち医薬品の「成分」、「分量」、「用法」、「用量」、「効能」及び「効果」について、両処分を比較して判断すべきであるとしています。そして、特許庁における審査基準も同最高裁判決に沿って改訂されています。
このように、「パシーフカプセル30mg知財高裁判決」を契機として、審査実務では、拒絶要件の判断において延長特許権の効力を考慮しない運用へと転換しました。さらに、「ベバシズマブ最高裁判決」により、「成分」、「分量」、「用法」、「用量」、「効能」及び「効果」をもって物の特定要素として捉え、これらを異にする医薬品ごとに、特許権の存続期間延長の可否及びその期間の長短を個別に審査・査定する運用となりました。これは、物の特定要素を、「有効成分」、「効能」及び「効果」としていた従前の特許庁実務と比較すると、延長登録の範囲・単位が「短冊化」されたものといえます。
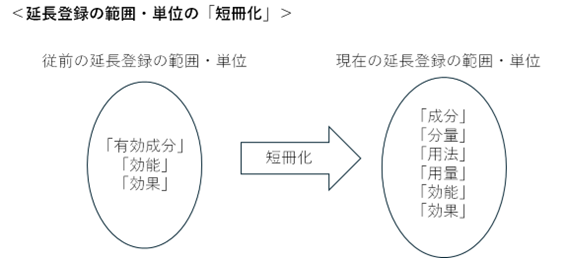
延長された特許権の効力の及ぶ範囲について
延長された特許権の効力の及ぶ範囲の解釈
存続期間の延長を受けた特許権の効力が被告製品に及ぶかを判断するにあたっては、下図のとおり二段階のステップを踏むことになります。第1ステップとして、被告製品が特許発明の技術的範囲に属するかを判断します。被告製品が特許発明の技術的範囲に属すると判断された場合には、第2ステップとして、特許法第68条の2に基づき、延長された特許権の効力が被告製品に及ぶかを判断します。
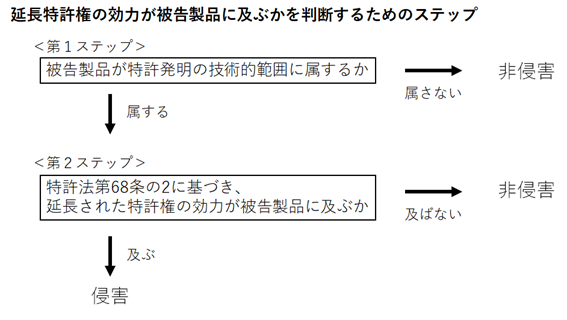
前述のとおり、特許法第68条の2は、存続期間の延長を受けた特許権の効力が及ぶ範囲を「政令で定める処分の対象となつた物」に限定しており、さらに当該物の「用途」が定められている場合は、当該用途に使用されるその物にまで限定されます。同条における「物」および「用途」の意義については、かつて、「物」は「有効成分」を、「用途」は「効能・効果」を意味すると解されてきました。しかし、このような解釈は、近年、ドラッグ・デリバリー・システムなど、有効成分や効能・効果以外に特徴を有する医薬発明にも特許権が付与されるようになったことから、批判を受けるようになりました。
このような状況の下で、前述の「ベバシズマブ知財高裁判決」において、知財高裁は、傍論ながら、延長特許権の効力範囲について、特許法第68条の2における「物」を「成分(有効成分に限らない)」、「用途」を「効能・効果」及び「用法・用量」と解し、従前の「物」や「用途」の解釈とは異なる考え方を示しました。さらに、その後、いわゆる「オキサリプラチン知財高裁判決」(知財高判大合議平成29年1月20日平成28年(ネ)第10046号)において、知財高裁は、下図に示すとおり、延長特許権の効力における「物」とは、政令処分で定められた「成分,分量,用法,用量,効能及び効果」によって特定されるとしました。その上で、延長特許権の効力は、特許発明の内容に基づき、その内容との関連で、政令処分で定められた当該「物」と対象製品との技術的特徴及び作用効果の同一性を比較検討して、当業者の技術常識を踏まえて判断すべきであるとの判断を示しました(詳しくは、こちらの記事もご覧ください)。

事案の概要
事案
・概要
本事案は、特許第4889219号「腹部不快感の処置のためのプロスタグランジン誘導体」(以下「本件特許1」といいます。)及び特許第4332353号「15-ケト-プロスタグランジン類を含む薬物誘発性便秘処置用組成物」(以下「本件特許2」といいます。)の専用実施権者である原告が、本件特許1、2に係る特許権(それぞれ「本件特許権1」、「本件特許権2」といい、これらをまとめて「本件特許権」といいます。)の存続期間が延長されたことを前提に、被告が被告製品の生産、譲渡等をした行為が、延長された本件特許権を侵害すると主張し、その差止めを求めたものです。なお、本件特許権の特許権者は、原告補助参加人として本件訴訟に参加しています。
また、本件では、本件特許1に係る特許権差止請求事件(令和7年(ワ)第10786号)と、本件特許2に係る特許権差止請求事件(令和7年(ワ)第10790号)とが、弁論併合されて審理されています。
・本件特許1及びその延長登録
本事案において、本件特許1については、請求項1と請求項14に係る発明について、被告製品が当該発明の構成要件を充足するかが問題となりました(以下、本件特許1の請求項1に係る発明を「本件発明1-1」、請求項14に係る発明を「本件発明1-14」といい、これらを総称して「本件各発明1」といいます。)。
また、本件特許1に対しては、2回の延長登録がなされています(以下、1回目の延長登録を「本件延長登録1-1」、2回目の延長登録を「本件延長登録1-2」といいます。)。
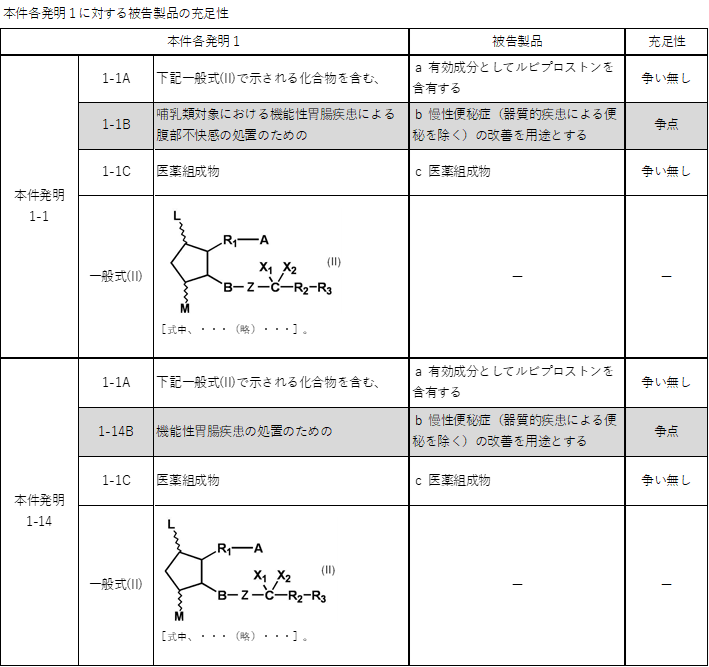
本件各発明1の構成要件の分説と、本件延長登録1-1及び1-2の内容をまとめると以下のとおりです。
なお、本件延長登録1-2については、被告により延長登録の無効審判請求がなされています。
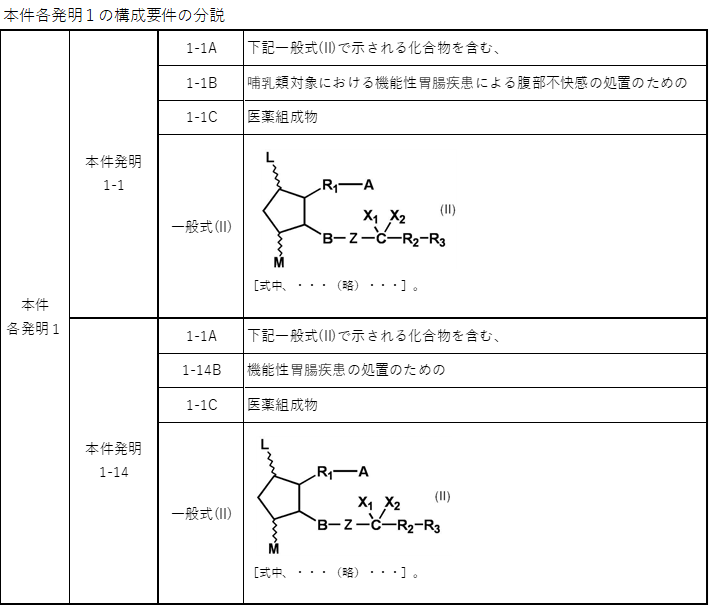
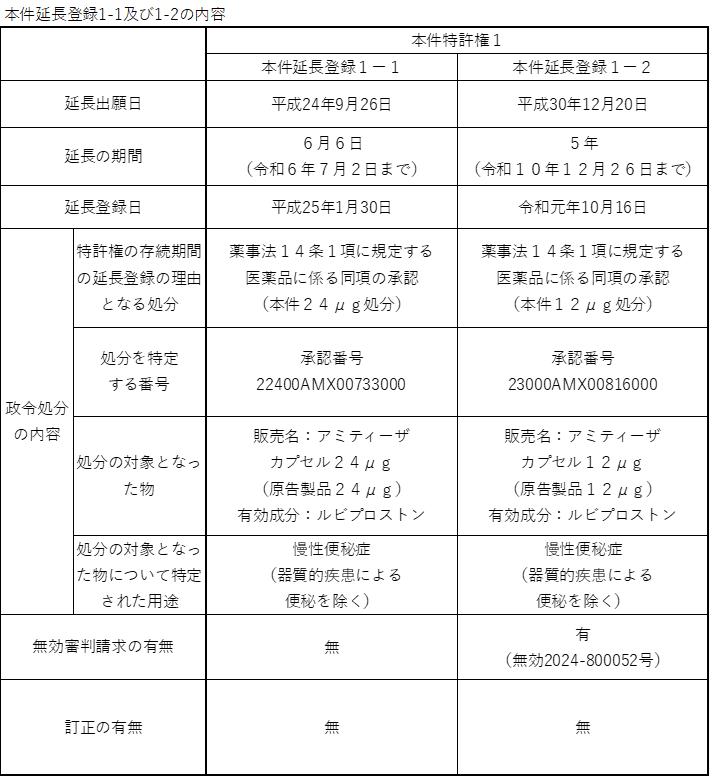
・本件特許2及びその延長登録
本事案において、本件特許2については、訂正前の請求項1および訂正後の請求項4について、被告製品が当該発明の構成要件を充足するかが問題となりました(以下、本件特許2における訂正前の請求項1に係る発明を「本件訂正前発明2」、訂正後の請求項4に係る発明を「本件訂正後発明2」といい、これらを総称して「本件各発明2」といいます。)。
また、本件特許2に対しては、2回の延長登録がなされています(以下、1回目の延長登録を「本件延長登録2-1」、2回目の延長登録を「本件延長登録2-2」といいます。)。
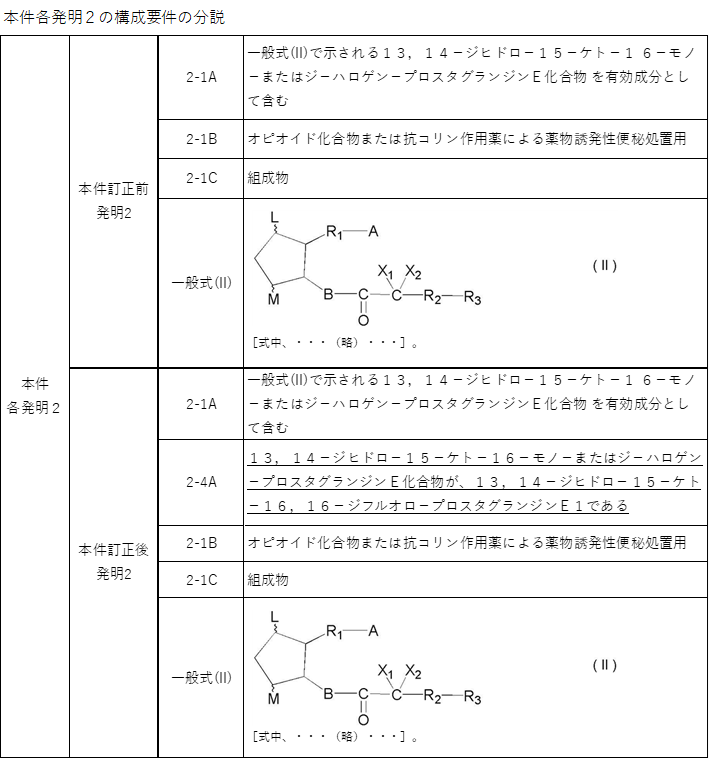
本件各発明2の構成要件の分説と、本件延長登録2-1及び2-2の内容をまとめると以下のとおりです。
なお、本件延長登録2-2に対しては、被告により延長登録の無効審判請求がなされています。これに対し、本件特許2の特許権者(本件の補助参加人)は、請求項1~8について訂正請求を行っており、本件訂正後発明2は、当該訂正に係るものです(下線部は訂正箇所を示します)。特許庁は、当該訂正を認めた上で、無効審判請求は成り立たないと判断するとともに、訂正により削除された請求項2及び3に係る審判請求については却下する旨の審決をしています。

・被告製品について
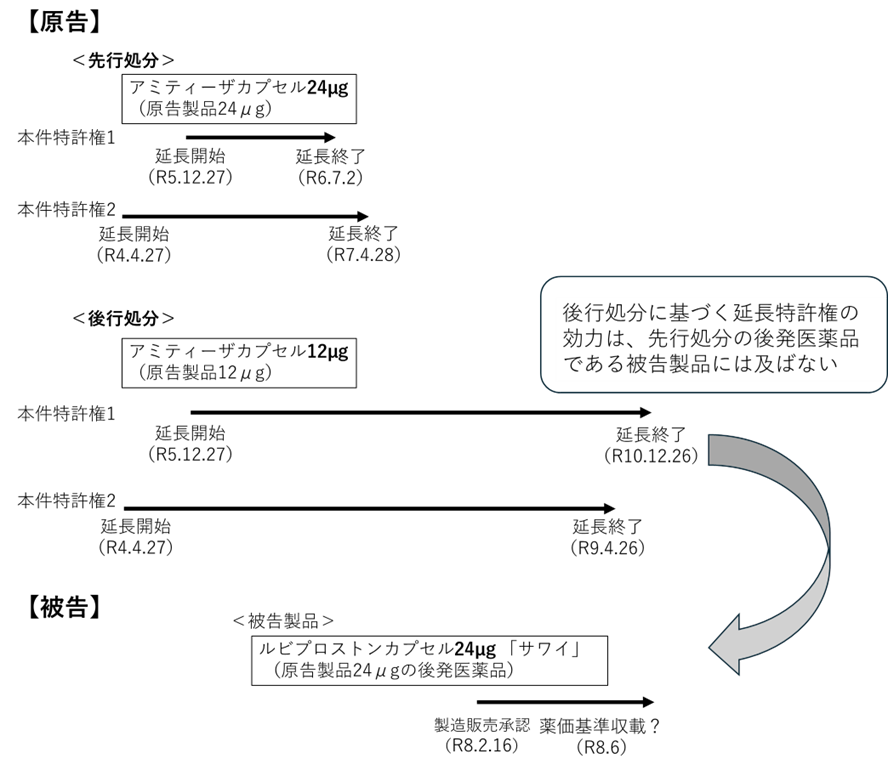
被告は、令和5年2月24日、原告製品24μgの後発医薬品として、下記構成の被告製品(ルビプロストンカプセル24μg「サワイ」)についての製造販売承認申請をしました。なお、被告製品は、令和7年8月には製造販売承認がされませんでしたが、令和8年2月に製造販売承認がされた場合には、同年6月に薬価基準に収載されることが見込まれていました(令和8年2月16日に製造販売承認済み)。
a 有効成分としてルビプロストンを含有する
b 慢性便秘症(器質的疾患による便秘を除く)の改善を用途とする
c 医薬組成物
被告製品の構成a及びcは、本件各発明1のうち構成要件1-1A及び1-1C、本件各発明2のうち構成要件2-1A、2-4A及び2-1Cをそれぞれ充足することについて争いはありませんでした。一方、その余の構成要件充足性(被告製品の構成bが、本件各発明1のうち構成要件1-1B及び1-14B、本件各発明2のうち構成要件2-1Bをそれぞれ充足するか否か)が争点となりました(後述の争点1)。

・2回の延長登録の関係について
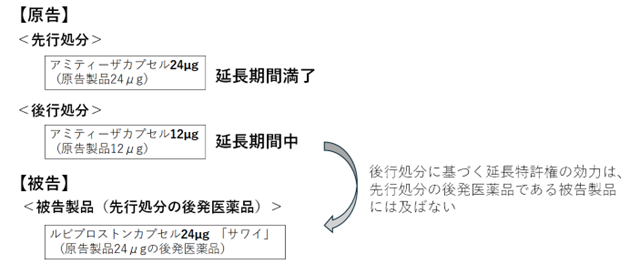
本件特許権1及び本件特許権2については、いずれも2回の延長登録がされています。すなわち、1回目の延長登録(本件延長登録1-1及び2-1)は、原告製品24μgに対する処分に基づくものであり、その延長期間は既に満了しています。これに対し、2回目の延長登録(本件延長登録1-2及び2-2)は、原告製品12μgに対する処分に基づくものであり、本判決当時も延長期間中にありました。
したがって、本件は、先行処分(24μg)に基づく延長登録が既に終了している一方で、当該先行処分とは分量のみが異なる後行処分(12μg)に基づく延長登録が継続しているという状況にあります。
本判決の判断
争点概要
本件の争点は以下のとおりです。
争点1:被告製品は本件各発明1及び同2の技術的範囲に属するか
争点2:本件延長登録1-2及び同2-2により存続期間が延長された本件特許権1及び同2の効力は被告製品の生産・譲渡等に及ぶか
争点3:本件延長登録1-2及び同2-2に無効理由があるか
争点4:差止め等の必要性
なお、裁判所は、争点1及び2において非侵害という判断に至ったため、争点3及び争点4については判断を示しませんでした。
裁判所の判断の概要
裁判所は、被告製品は、本件各発明1及び同2のいずれの技術的範囲にも属するが(争点1)、本件延長登録1-2及び同2-2によって存続期間を延長された本件特許権1及び同2の効力は、いずれも被告製品の生産・譲渡等に及ばないと判断しました(争点2)。
すなわち、本件においては、特許発明の技術的範囲の属否に関する第1ステップはクリアしたものの、延長特許権の効力に関する第2ステップをクリアできず、延長特許権の侵害は成立しないと判断されたものです。
争点1(被告製品は本件各発明1及び同2の技術的範囲に属するか)の判断
裁判所は、延長特許権の効力が被告製品に及ぶかを判断するにあたり、まず、第1ステップとして、被告製品が特許発明の技術的範囲に属するか否かを検討しました。
まず、裁判所は、技術常識等に照らせば、被告製品における用途である「慢性便秘症(器質的疾患による便秘を除く)」は機能性便秘症に含まれ、かつ、当該機能性便秘症は「機能性胃腸疾患」に含まれること、さらに便秘は「腹部不快感」を伴うことから、被告製品は本件各発明1の構成要件を充足すると判断しました。
被告製品は、「慢性便秘症(器質的疾患による便秘を除く)の改善を用途とする」(構成b)ものである・・・が、技術常識・・・に照らせば、器質的疾患による便秘を除く慢性便秘症の一態様として、機能性消化管疾患であるところの便秘(機能性便秘症)をも用途としていると解される上、一般に機能性消化管疾患は機能性胃腸疾患と同義といえること、便秘が腹部不快感を伴うものであることも踏まえれば、「哺乳類対象における機能性胃腸疾患による腹部不快感の処置のための」及び「機能性胃腸疾患の処置のための」との各構成要件を充足する。
つづいて裁判所は、技術常識や被告製品の添付文書等に照らせば、被告製品における用途である「慢性便秘症(器質的疾患による便秘を除く)」の一態様として、オピオイド化合物や抗コリン薬等の薬剤性便秘も用途とすることから、被告製品は本件各発明2も充足すると判断しました。
被告製品は、「慢性便秘症(器質的疾患による便秘を除く)の改善を用途とする」(構成b)ものである…が、技術常識…及び被告製品の添付文書案…に照らせば、器質的疾患による便秘を除く慢性便秘症の一態様として、抗コリン薬、抗うつ薬、オピオイド系薬、Ca拮抗薬などの薬剤性便秘をも用途としていると解されるところ、「オピオイド化合物または抗コリン作用薬による薬物誘発性便秘処置用」との構成要件を充足する。
以上により、裁判所は、被告製品は、本件各発明1及び同2のいずれの技術的範囲にも属すると判断しました。
争点2(本件延長登録1-2及び同2-2により存続期間が延長された本件特許権1及び同2の効力は被告製品の生産・譲渡等に及ぶか)の判断
・概要
裁判所は、延長特許権の効力が被告製品に及ぶかの判断における第2ステップにおいて、特許法第68条の2に基づき、本件延長登録1-2及び同2-2により延長された特許権1及び同2の効力が被告製品の生産・譲渡等に及ぶか否かを検討しました。
・問題の所在
裁判所は、争点2に関する問題の所在を、次の二点に整理しました。
①分量を24μgとする被告製品が、本件12μg処分の対象となった物である原告製品12μgと同一であるとして特許権の効力が及ぶといえるか。
②本件24μg処分を理由とする本件延長登録1-1の延長期間は既に終了している中で、これと分量を同じくする被告製品に対し、本件12μg処分という別の理由で延長登録された本件特許権1の効力が及ぶといえるか。
上記問題点を踏まえ、裁判所は、まず延長された特許権の効力の解釈に当たっては、特許権の存続期間の延長登録制度全体に対する考察(延長登録の範囲・単位、特許権者と第三者との衡平の観点)が、問題の性質上不可欠であるとの考えを示しました。
つまるところ、特許法68条の2の・・・「物」との同一性の範囲をどのように解するかの法律論に収れんされる問題ではあるが、その解釈にあたっては、特許権存続期間の延長登録制度全体に対する考察、すなわち、延長登録の範囲・単位をどのように解すべきかにも立ち返りつつ、存続期間を延長された特許権の効力範囲をどのように解することが、延長特許の範囲・単位についての解釈と整合的で、特許権者と第三者との衡平にも適うものであるかという観点で検討することが、本問題の性質上不可欠といえる。
・延長登録の範囲・単位
裁判所は、延長された特許権の効力を解釈するに際して、まず、延長登録の範囲・単位について検討しました。
裁判所は、延長登録の範囲・単位について、従前の特許庁実務における取扱いと比較しつつ、ベバシズマブ最高裁判決によりその範囲・単位が「短冊化」されたことに着目した上で、延長された特許権の効力範囲についても、当該短冊化された範囲内にとどまるものと解するのが相当であるとの考えを示しました。
その意味するところは、従前の特許庁実務と対比することでより明瞭になる。すなわち、従前の特許庁実務は、有効成分と効能及び効果を同じくする複数の医薬品については、例えば、分量を異にし、薬機法に基づく製造販売承認の審査上は別の医薬品として扱われるものであったとしても、1つの医薬品を対象とする政令処分を理由に延長登録がされれば、その後に別の医薬品を対象とする政令処分を理由とする別の延長登録は認めないとするものであった。このような解釈運用は、条文文言(現行特許法67条の7第1項1号)との整合性に加え、実質論としても、後行処分に係る医薬品について、特許権存続中の実施可能期間が存続期間延長登録制度の意図するところよりも短くなってしまうという問題があったと考えられるが、その点はおくとして、存続期間を延長された当該特許権の効力としては、有効成分と効能及び効果を同じくする医薬品であれば、例えば、分量を異にしても「物」(現行特許法68条の2)として同一であり、広く効力範囲に含まれると解するのが整合的ということになる。言い換えれば、そのように特許権の効力範囲を広く解さなければ、上記のように延長登録出願に係る範囲・単位を広く扱い、有効成分と効能及び効果を同じくする限り、別途の延長登録を認めないとする解釈運用を正当化することは困難であったと考えられる。他方で、ベバシズマブ最高裁判決によって定立されたというべき前記のような延長登録の範囲・単位は、薬機法に基づく医薬品の製造販売承認の審査と全く同一までではないものの、実質においてはこれと近似したものとなり、成分、分量、用法、用量、効能及び効果をもって、物としての特定要素とし、これを異にする医薬品については、それぞれごとに、特許権の存続期間延長の可否及びその期間の長短を審査、査定することとなる。これは、延長登録の範囲・単位について、薬機法に基づく製造販売承認に概ね近似する単位とし、従前の特許庁実務に比べると相当にいわば短冊化したものといえ、存続期間延長登録制度のもとでの特許権者と第三者との衡平を、よりきめ細やかに行うことを可能にするものと捉えることができる。そして、このような存続期間延長登録制度の短冊化に照らして考えると、延長された特許権の効力範囲についても、このような短冊化された範囲内にとどまると解するのが整合的とはなる。・・・
・特許法68条の2の文言からの考察
続いて裁判所は、延長特許権の効力について、特許法68条の2の文言からの考察を行っており、オキサリプラチン知財高裁判決と同様の基準を示しました。すなわち、延長登録の理由となった政令処分の対象となった物と、権利行使の対象製品とが、特許法第68条の2の規定における「物」、すなわち、政令処分上で定められた成分、分量、用法、用量、効能及び効果をもって特定される物として実質同一の範囲に属する場合は、当該範囲において延長特許権の効力が及ぶことを確認しました。
・・・特許法68条の2の規定における「物」も、政令処分上で定められた成分、分量、用法、用量、効能及び効果をもって特定されると解される。・・・特許権者と第三者との衡平の観点から、延長登録の理由となった政令処分の対象となった物と、権利行使の対象製品との間に、上記特定要素につき何らかの異なる部分があったとしても、当該部分が僅かな差異又は全体的にみて形式的な差異にすぎないときは、権利行使の対象製品は、延長登録の理由となった政令処分の対象となった物と実質同一として、延長された特許権の効力が及ぶと解することが相当である・・・僅かな差異又は全体的にみて形式的な差異かどうかは、特許発明の内容に基づき、その内容との関連で、政令処分において定められた「成分、分量、用法、用量、効能及び効果」によって特定された「物」と対象製品との技術的特徴及び作用効果の同一性を比較検討して、当業者の技術常識を踏まえて判断すべきと解される(オキサリプラチン知財高裁判決参照)。
・総合的考察
以上の「延長登録の範囲・単位」及び「特許法第68条の2の文言」の検討に加え、特許権者と第三者との衡平の観点から、裁判所は、延長登録出願時における延長登録の範囲・単位と、延長特許権の効力範囲とは、必ずしも一致するものではなく、延長特許権の効力範囲は、延長登録の範囲・単位よりも一定の広がりを有し得ると解しました。そして、当該広がりは、存続期間の延長登録の範囲・単位と抵触しないという制約の中で解釈されるべきであるとの考えを示しました。
・・・延長登録出願の段階での延長登録の範囲・単位と、存続期間が延長された特許権の効力範囲は、規範やその背景事情を異にするもので、両者の範囲は必ずしも一致するものではなく、むしろ、一般的にいえば、後者の方が広がりをもった範囲を有するといえる。しかしながら、延長登録の範囲・単位とその結果存続期間が延長された特許権の効力範囲は、存続期間の延長登録制度全体の中で、整合的に解釈運用され、相互に調和することで、初めて特許権者と第三者との衡平という同制度の目的の実を果たすことができるというべきであるところ、特許権の効力範囲については、前記イ及びウで検討したところを総合考慮し、実質同一といえる範囲で広がりを有するとはいえ、その広がりは、存続期間の延長登録の範囲・単位と抵触しないという制約の中で解釈されるべきものといえる。
その上で、先行処分の対象とする物と成分、分量、用法、用量、効能及び効果として同一の物は、後行処分に基づく延長登録の対象物との関係では実質同一とはいえず、その生産・譲渡等にまで延長特許権の効力は及ばないと解しました。
すなわち、医薬品に係る同一の特許権について、複数の政令処分を理由とする延長登録がされている場合、後れて延長登録された特許権の効力範囲は、前記ウで説示の規範のもと一定の広がりを有するものではあるものの、少なくとも、先行する延長登録の理由となった政令処分の対象とする物と成分、分量、用法、用量、効能及び効果として同一の物は、後行する延長登録の理由となった政令処分の対象とする物と実質同一ではなく、その生産・譲渡等にまでは効力が及ばないものとして解されるべきである。
このように、裁判所は、後行処分にかかる延長特許権の効力は、先行処分に係る医薬品と同一の医薬品には及ばない旨を明確に示しました。
そして裁判所は、その理由として、仮に効力が「及ぶ」と解した場合には、存続期間延長制度の趣旨を大きく損なうことになり、当該範囲に特許権の効力を及ぼす実質的正当性を欠くことになることを挙げました。
仮に、後れて延長登録された特許権の効力が、前記ウの規範のもと、先行する延長登録の理由となった政令処分の対象とする物と成分、分量、用法、用量、効能及び効果として同一の物の生産・譲渡等にまで及ぶとすれば、先行する存続期間の延長の方が短かった場合において、その対象とする物の第三者による実施が、存続期間延長制度が規律する以上の期間にわたって禁じられることになる。このような帰結は、延長登録出願段階での範囲・単位を成分、分量、用法、用量、効能及び効果で短冊的に区分けし、特許権者と第三者との衡平を、その範囲・単位できめ細やかに調整しようとする存続期間延長制度の趣旨を大きく損なうものであるとともに、既に延長期間が終了した延長登録の理由となった政令処分の対象とする物と成分、分量、用法、用量、効能及び効果として同一の物に対して特許権の行使を受けるということは、第三者の予期を期待できるものではなく、特許権の効力を及ぼす実質的正当性に欠けるものともいえる。
・本件へのあてはめ
裁判所は、まず、原告製品12μgと被告製品24μgとの関係について検討し、両者は分量に差異があるものの、僅かな差異又は全体的にみて形式的な差異と見る余地があることは否定できないと解しました。
・・・本件12μg処分の対象となった原告製品12μgと被告製品は、分量こそ12μgと24μgという 違いがあるものの、成分、用法、用量、効能及び効果は同一である上、本件各発明1の内容に照らせば、上記分量の差異が技術的特徴や作用効果に違いをもたらすとはいい難いと考えられるところ、上記差異そのものの評価としては、前記ウの規範でいうところの僅かな差異又は全体的にみて形式的な差異と見る余地があることは否定できない。
しかしながら、裁判所は、被告製品は、先行処分の対象となった原告製品24μgと成分、分量、用法、用量、効能及び効果が同一の物であること等を理由に、被告製品24μgは原告製品12μgと実質同一であるとは認められず、その生産・譲渡等にまで延長特許権の効力は及ばないと判断しました。
・・・被告製品は、まさに先行する本件延長登録1-1の理由とされた本件24μg処分の対象となった原告製品24μgと成分、分量、用法、用量、効能及び効果が同一の物であるところ、上記延長登録に係る延長期間は既に終了したものである。後行する本件延長登録1-2によって存続期間を延長された本件特許権1の効力は、その延長登録の理由となった本件12μg処分の対象である原告製品12μgと分量のみを異にする医薬品を実質同一の範囲に含むものとして一定の広がりを有するとまではいえるものの、前記エでの説示に照らせば、原告製品24μgとの同一性に係る上記一事をもって、少なくとも、被告製品は原告製品12μgと実質同一ではなく、その生産・譲渡等にまで効力は及ばないというべきである。
また、裁判所は、原告及び補助参加人(以下「原告ら」といいます。)の主張を認めた場合には、存続期間延長制度の趣旨及び想定とは異なり、失われた期間の回復を超えて、延長登録の理由となった政令処分の対象とする物についての実施権の専有を認めるに等しく、実質において、特許権者と第三者との衡平を損なう結果を招く実質的な妥当性・衡平を欠くとしました。
・・・なお、この点で、仮に原告及び補助参加人の主張を認めた場合、・・・本件延長登録1-2によって存続期間が延長された本件特許権1の効力として、さらに令和10年12月26日までの間、被告製品その他原告製品24μgと成分、分量、用法、用量、効能及び効果を同じくする物の第三者による生産・譲渡等を差し止めることができることになる。これは、本来、政令処分を受けるまでの失われた期間に限り、存続期間の延長を許容する存続期間延長制度の趣旨、想定とは異なり、失われた期間の回復を超えて、延長登録の理由となった政令処分の対象とする物についての実施権の専有を認めるに等しく、実質において、特許権者と第三者との衡平を損なう結果を招くものといえる。
(オキサリプラチン知財高裁判決に関する原告らの主張について)
裁判所は、原告らが依拠するオキサリプラチン知財高裁判決に関する主張を採用しませんでした。すなわち、原告らは、被告製品が同判決の示す類型④(政令処分で特定された「分量」は異なるけれども、「用法、用量」も併せてみれば、同一であると認められる場合)に該当し、原告製品12μgと実質同一であるため、延長特許権の効力が及ぶと主張しましたが、裁判所はこれを退けました。
その理由として、裁判所は、延長特許権の効力範囲は、存続期間の延長登録制度全体との整合的解釈の観点から、延長登録の範囲・単位と抵触しないという制約の中で解釈されるべきである、とした上で、原告らの主張は、このような制約に対する考慮を欠いたものであると指摘しました。
これに対し、原告及び補助参加人は、オキサリプラチン知財高裁判決が定立した実質同一の規範に照らせば、本件延長登録1-2によって存続期間を延長された本件特許権1の効力は、被告製品の生産・譲渡等にも及ぶ旨主張する。
しかし、前記イないしエで説示したとおり、存続期間を延長された特許権の効力範囲については、延長登録の理由とした政令処分の対象となった物と実質同一の物の生産・譲渡等にまで及ぶものではあるものの、存続期間の延長登録制度全体の中での整合的解釈として、延長登録の範囲・単位と抵触しないという制約の中で解釈されるべきものであるところ、原告の主張は、この点への考慮を欠いたものというほかない。
(ベバシズマブ知財高裁判決に関する原告らの主張について)
裁判所は、原告らが依拠するベバシズマブ知財高裁判決に関する主張を採用しませんでした。
まず、原告らは、同判決の傍論部分を引用し、存続期間の延長登録が複数並立している場合には、1つの延長登録に係る特許権の効力が、他の延長登録の理由となった政令処分の対象とした物と同一の物の生産・譲渡等に及ぶことは、特許法制上想定されていると主張しました。
原告及び補助参加人は、ベバシズマブ最高裁判決の原判決であるベバシズマブ知財高裁判決の、以下の部分を引用しつつ、存続期間の延長登録が複数並立している場合に、1つの延長登録に係る特許権の効力が、他の延長登録の理由となった政令処分の対象とした物と同一の物の生産・譲渡等に及ぶことは、特許法制上想定されている旨主張する。
「なお、政令で定める処分を受けることによって禁止が解除された特許発明の実施が、先行処分に基づき存続期間が延長された当該特許権の効力が及ぶ特許発明の実施の範囲に含まれるような場合は、重複して延長の効果が生じ得ることとなる。後行処分による延長期間が先行処分による延長期間より長い場合には、これに対応する期間、当該特許権の存続期間が延長されるが、当該期間については、当該特許発明の実施が禁止されていた部分があることに照らすと、上記のように解することに何ら不合理な点はない。」
裁判所は、ベバシズマブ知財高裁判決の趣旨について検討し、重複して延長の効果が生じ得ること自体は認めました。
まず、上記説示は、先行する政令処分によって存続期間が延長された特許権の効力範囲が、後行する政令処分の対象とする物と同一の物の生産・譲渡等に及び得ること、そのように解したとして特段不合理な点はないということを述べるものである。すなわち、先行する政令処分とこれに基づく延長登録の際には、まだ後行の延長登録がされているわけではなく、延長登録の並列状態及びこれに伴う効力範囲の制約がない中で延長登録がされることになるため、後行する政令処分の対象とする物と同一の物の生産・譲渡等を包含するように効力範囲が及ぶ可能性があるといえる。また、結果として、後行する政令処分の対象とする物の実施については、観念上、重複して延長の効果が生じ得ることにはなるが、後行の延長登録による延長期間は、元々当該物の実施が薬機法上禁止されていた期間に対応するものにとどまるから、延長登録制度の趣旨、想定を超える期間にわたって実施権の専有が得られるわけでもない。
一方、裁判所は、これとは逆の方向性、つまり、後行処分に基づく延長特許権の効力が、先行処分の対象とする物に及ぶかについては、ベバシズマブ知財高裁判決は何ら説示するものではなく、実際上も利害状況が大きく相違すると述べました。そして、このような観点から、少なくとも、先行処分の対象とする物と成分、分量、用法、用量、効能及び効果が同一の物の生産・譲渡等にまで、後行処分に基づく延長特許権の効力は及ばない、と解し、原告の主張を退けました。
しかし、これと逆の方向性、つまり、後行する政令処分によって存続期間が延長された特許権の効力範囲が、先行する政令処分の対象とする物と同一の物の生産・譲渡等にまで及び得るかについては、上記説示部分は何ら言及するものではなく、実際上も利害状況が大きく相違する。すなわち、後行する延長登録の際には、先行する延長登録(少なくとも、その出願)が存在するのであって、まさに前記エの説示が想定する状況であり、後行する延長登録によって存続期間が延長された特許権の効力範囲につき、先行する延長登録との整合性を考慮して解釈しなければ、延長登録制度全体の趣旨を損ねることになるところ、少なくとも、先行する政令処分の対象とする物と成分、分量、用法、用量、効能及び効果が同一の物の生産・譲渡等にまで効力は及ばないものと解される。
(残された法的問題について)
裁判所は、先行する政令処分に基づく延長登録が存在しない場合において、後行処分に基づく延長特許権の効力範囲をどのように解すべきかという法的問題がなお残されていることを指摘しました。もっとも、この点は本件とは事案を異にし、かつ、本件における判断を左右するものではないとして、裁判所はこれ以上の検討は行わず、その判断も示しませんでした。
なお、以上の説示を前提としても、先行する政令処分(本件でいえば、本件24μg処分)を理由とした延長登録をしていない場合に、後行する政令処分(本件でいえば、本件12μg処分)を理由とする延長登録によって延長された特許権の効力範囲をどのように解するかという法的問題が残されている。この点、本件のように、先行する政令処分を理由とした延長登録をしている場合との均衡を損ねることのないような解釈が検討されるべきではあるが、本件とは事案を異にするもので、これ以上詳細に検討することはしない。いずれにしても、そのような法的問題の存在は、本件の事実関係のもとで、存続期間の延長登録制度全体との整合性や権利者と第三者との衡平の観点から採られた当裁判所の解釈を左右するものではなく、むしろ、このような解釈も前提に、次の応用的な法的問題として、整合的な法解釈が検討されるべきものといえる。
まとめ
以上のとおり、争点1、2に関する裁判所の判断をまとめると下記のとおりとなります。
争点1:被告製品は本件各発明1及び同2の技術的範囲に属する。
争点2:延長された特許権1、2の効力は、被告製品の生産・譲渡等に及ばない。
コメント
本判決の特徴は、後行処分に基づく延長特許権の効力範囲を解釈するに当たり、既に延長期間が満了した先行処分に係る延長登録の範囲・単位との関係を考慮し、その効力範囲を限定的に解釈した点にあります。すなわち、延長特許権の効力が及ぶ「実質同一」の範囲について、オキサリプラチン知財高裁判決が示した枠組みを前提としつつも、これを延長登録の範囲・単位と抵触しないという制約の中で解釈すべきであるとした点に意義があります。
オキサリプラチン知財高裁判決は、特許法68条の2の規定における「物」を、政令処分において定められた成分、分量、用法、用量、効能及び効果という6要素によって特定される物ととらえ、その実質同一の範囲において、延長特許権の効力が及ぶとするとともに、第1類型から第4類型を例示しました。
本件では、先行処分(12μg)に基づく延長登録期間が既に満了した後、当該先行処分とは前記6要素のうち「分量」のみが異なる後行処分(24μg)に基づく延長登録がされた特許権の効力が、「分量」は後行処分(24μg)とは異なるものの、先行処分とは一致する被告製品(12μg)に及ぶかが問題となりました。
この点について、オキサリプラチン知財高裁判決が示した「実質同一」の判断枠組みを形式的に適用すれば、後行処分に係る原告製品と被告製品とは「分量」のみが異なるにとどまり、第4類型(「分量」は異なるけれども、「用法、用量」も併せてみれば同一であると認められる場合)に該当し得るため、両者は実質同一であり、延長特許権の効力が及ぶと解する余地もあると思われます。
しかしながら、本判決は、延長特許権の効力範囲は、延長登録制度全体の整合性、とりわけ延長登録の範囲・単位との関係を踏まえて解釈すべきであるとした上で、先行処分の対象とする物と成分、分量、用法、用量、効能及び効果として同一の物は、後行処分の対象とする物と実質同一ではなく、効力は及ばないと判断しました。
このように本判決は、後行処分に係る原告製品と被告製品との間に、前記6要素の観点からみて僅かな差異又は全体的にみて形式的な差異であっても、当該被告製品が先行処分に係る原告製品と前記6要素において同一である限り、後行処分に基づく延長特許権の効力は及ばないことを示した点に意義があるといえます。
もっとも、本件については原告により控訴が提起されていることから、上記問題の帰趨については、今後の判断動向を注視する必要があります。
本記事に関するお問い合わせはこちらから。
(文責・竹下)
- 投稿タグ
- アミティーザ, 医療機器等の品質, 医薬品, 存続期間が延長された特許権の効力, 延長登録, 有効性及び安全性の確保等に関する法律, 特許法, 知的財産高等裁判所, 薬機法












